在对蛋白的研究中,结构生物学是一个重要的范畴。其阐释生物大分子的三维结构。在结构生物学中,冷冻电镜是绝对主力。而由于冷冻电镜与晶体学方法无法看清楚蛋白质的柔性区域的结构,导致无法对蛋白质复合体进行建模。这些问题促进了质谱技术作为表征手段为结构生物学的发展提供帮助。
交联质谱法(Chemical cross-linking of proteins coupled with mass spectrometry analysis ,CXMS)是指利用化学交联剂将蛋白质或蛋白质复合体中空间距离足够接近的两个氨基酸通过共价键连接起来,酶切成肽段后用质谱鉴定出交联位点,从而获取低分辨度结构信息,帮助推断蛋白质在三维空间的折叠状态以及蛋白-蛋白相互作用的大致区域。
化学交联质谱技术是近年来发展起来的新方法,其利用化学交联剂处理蛋白质样品,将空间距离足够接近、可以与交联剂反应的两个氨基酸以共价键连接起来,然后利用基于质谱技术的蛋白质组学手段分析交联产物。这项技术有其独特的优势,如在于可以高通量地进行多种蛋白质的结构和相互作用分析,比传统方法速度快、信息产出规模大;通过交联剂的共价交联作用,可以固定原本不稳定的蛋白质相互作用,从而可以研究一大类容易解离的、结构松散的蛋白质复合物;相对于核磁共振、X 射线晶体衍射,交联质谱技术灵敏度高、对蛋白质性状要求低、需要样品绝对量小;可以进行体内交联,有助于研究体内蛋白质结构和相互作用;由于交联后的蛋白质先经过酶切之后才进行质谱分析,所以不受蛋白质本身的长度影响;使用不同臂长、不同反应基团的交联剂可以得到更多的蛋白质空间结构和相互作用信息。

Fig.1CXMS 技术流程图
CXMS技术是一项有挑战性的技术。其技术难点在于实验及数据分析两部分。实验部分的难点在于交联与质谱鉴定。最常用的交联剂是氨基反应的琥珀酰亚胺酯类,它们主要与K上的侧链氨基或蛋白的N端氨基进行交联反应。其次还有一些特色交联剂,如含有亲和基团的交联剂、在二级谱图中产生特殊碎裂信号的交联剂及同位素交联剂等。而由于交联后的多肽丰度低、交联形式复杂等问题,质谱鉴定也存在困难。我司基于nature methods文献[1]及配合pLink软件,对所鉴定的复杂的cross-linked谱图通过严格的FDR策略进行判别,以得到可信的蛋白cross-linked结果。
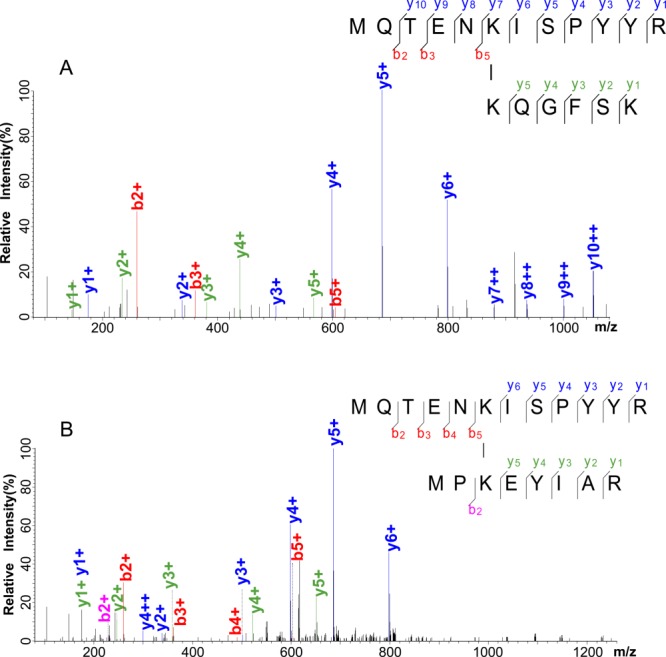
Fig.2 CXMS结果-谱图示例